avec l'anhydride carbonique CO2 O O M gCl + R C R utilisation de la carboglace, à
Publié le 26/02/2014

Extrait du document
avec l'anhydride carbonique CO2 O O M gCl + R C R utilisation de la carboglace, à -78°C + MgCl H O + R C H acide carboxylique C O O O obtention d'un carboxylate, moins réactif et qui, de plus est insoluble réaction avec les nitriles une cétone R' C R' N C R < Mg Cl R' N << MgCl R Liaison insuffisamment polarisée H2O R' NH C R H2O O C R imine instable dans l'eau 1 Un exemple d'utilisation d'organomagnésien : la synthèse du tamoxifène (Nolvadex®) modulateur sélectif des récepteurs des estrogènes utilisé sous forme orale dans le cancer du sein 2 Réactions particulières entre magnésiens et cétones encombrés O X C Mg H3 C C CH3 CH3 X X CH3 Mg C O CH3 C OH C O CH3 H2O C CH2 C H CH3 Mg H CH3 + H2C C CH3 H réduction en alcool secondaire oxydation en alcène 3 Autres Dérivés Organométalliques 5 métaux du groupe 1: électronégativité inférieure à celle du magnésium 1 H 2,1 Li 1 leur réactivité va augmenter avec le caractère électropositif croissant du métal (EN ) la réactivité des Organolithiens sera proche de celle des OHM Na 0,9 K 0,8 les sodiques et potassiques seront beaucoup plus réactifs, avec un caractère quasi-exclusif de bases fortes Rb 0,8 Cs 0,7 Fr 0,7 6 Organolithiens R-Li Généralités Li : électronégativité = 1 / Mg 1,2 gardent un caractère covalent marqué réactivité proche des OHM mais caractère basique plus marqué sont également des nucléophiles plus agressif structure plus complexe, formation de polymères mais dans les éthers, structure moins encombrée que les OHM Préparation H3C Br + 2 Li Bu-Br + 2 Li Et2O -20°C Et2O -20°C H3C Li + LiBr Bu-Li + LiBr solubles dans les alcanes : BuLI en solution dans l'hexane est commercial solubles (plus réactif) dans les éthers mais utilisables à basse température car ils commencent à cliver les éthers à température ambiante. réagissent violemment avec l'eau s'enflamment spontanément à l'air 7 Propriétés Propriétés basiques : réaction avec les dérivés à hydrogène mobile RCOOH, ArOH, ArSH,H2O, ROH, RSH, RCONHR', ArNH2, RNH2 ainsi que RC?CH ... décomposent les organolithiens comme les OHM comme les OHM, ils permettent d'obtenir des lithiens acétyléniques Li + R Bu C CH Bu H+ R C Li C + et également, dans certaines conditions, des lithiens éthyléniques tBu Li + H2C CH2 tBu H + H2C C Li pKa ~ 60 pKa ~ 36 Propriétés nucléophiles donnent lieu à toutes les réactions des OHM, avec quelques particularités avec les dérivés carbonylés donnent les réactions classiques, même avec les cétones encombrées
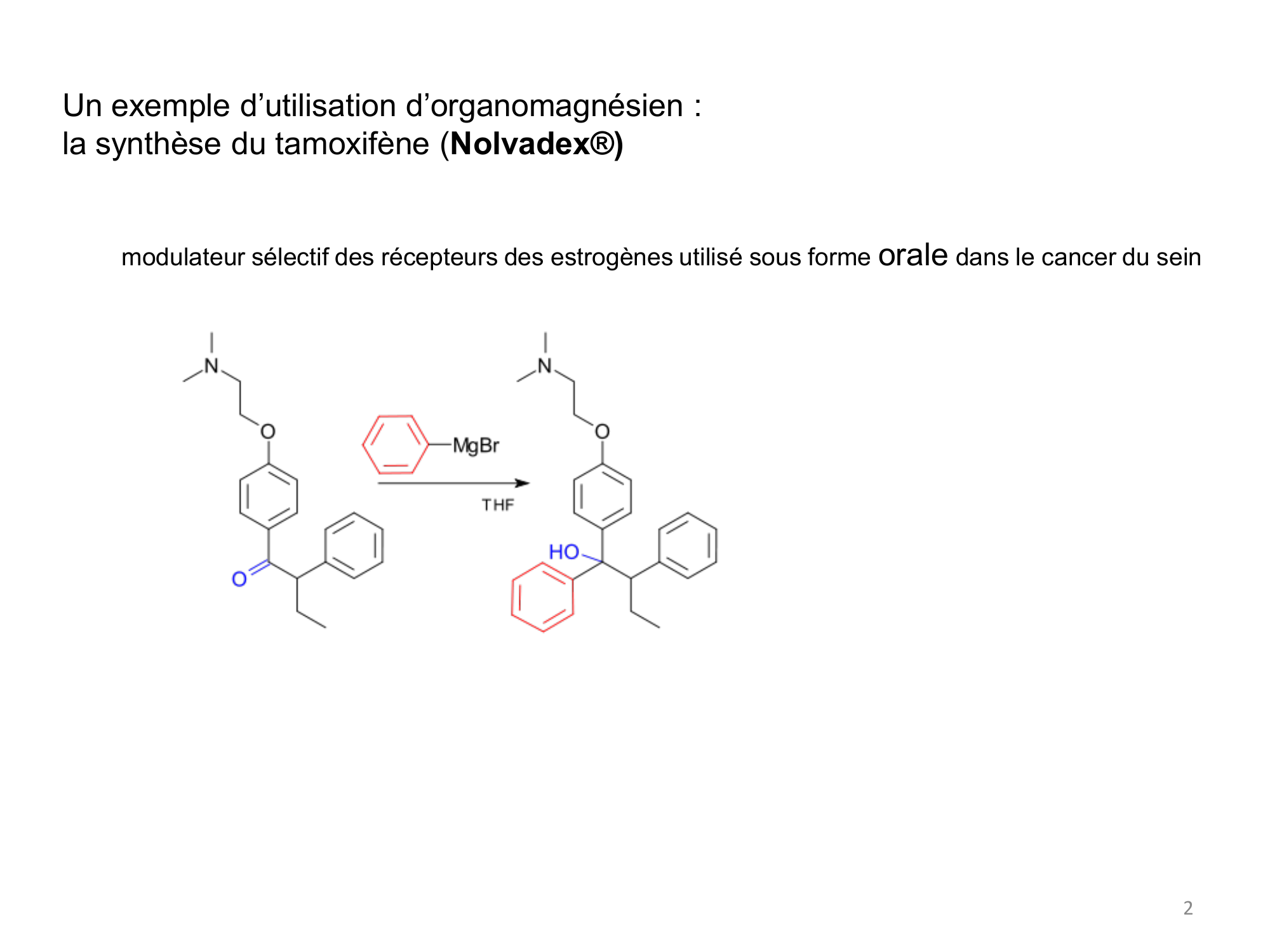
« 2 Un exemple d’utilisation d’organomagnésien : la synthèse du tamoxifène ( Nolvadex®) modulateur sélectif des récepteurs des estrogènes utilisé sous forme orale dans le cancer du sein. »
↓↓↓ APERÇU DU DOCUMENT ↓↓↓
Liens utiles
- DOMAINE PUBLIC - UTILISATION C.E. 29 janv. 1932, SOCIÉTÉ DES AUTOBUS ANTIBOIS, Rec. 117
- utilisation des prenthèses taille en allumettes et centimètres 2 allumettes et 3 cm 6
- Utilisation d'un personnage fictif
- Construire le symétrique d'une figure par rapport à un axe 2 Découvrir Au bord du canal o L'utilisation du papier calque sera privilégiée.
- utilisation des prenthèses Un ours mesure 6 allumettes et 2 cm.